Basierend auf den früheren „Froschzellen-Lebensrobotern“ (Xenobots) hat das wissenschaftliche Forschungsteam des Wyss Institute der Tufts University und der Harvard University erneut die Grenzen der Biotechnik erweitert und eine neue lebende Miniaturmaschine mit eigenem Nervensystem geschaffen – „Neurobots“. Es demonstrierte selbstorganisierte neuronale Netze und komplexere Verhaltensmuster und eröffnete ein neues Fenster zum Verständnis, wie Organismen funktionelle Strukturen aufbauen.
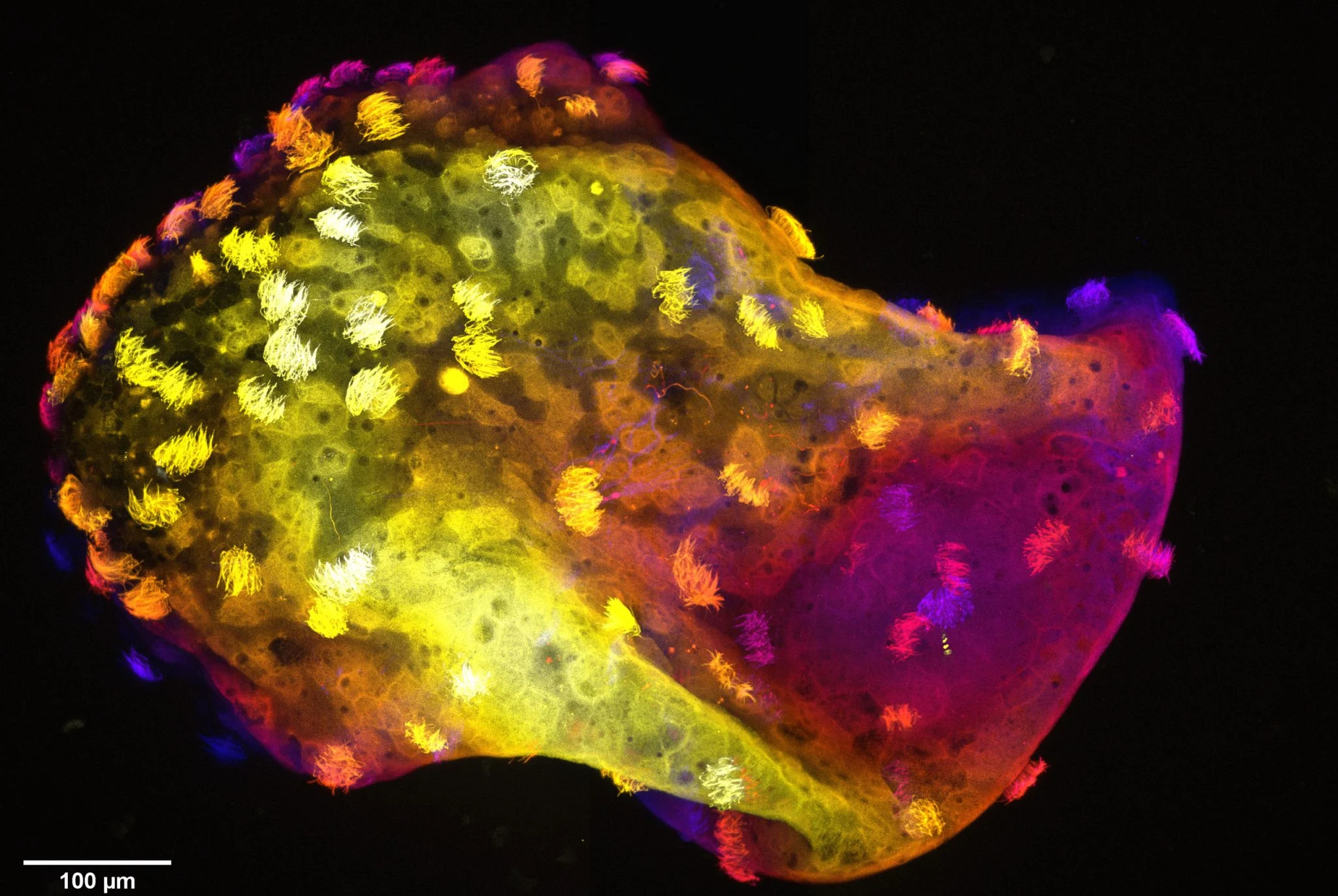
Bereits im Jahr 2020 verwendeten Forscher der Tufts University embryonale Zellen von Xenopus laevis, um „roboterähnliche“ biologische Strukturen im Mikrometermaßstab zu bauen – Froschzellroboter. Sie können sich im Wasser bewegen, sich selbst reparieren und sogar verstreute Zellen sammeln, um neue Individuen zu erzeugen. Die Strukturen, die sich vollständig aus lebenden Zellen ohne Gerüste oder genetische Modifikation zusammensetzen, leben etwa 9 bis 10 Tage und sind zum Überleben auf Nährstoffe angewiesen, die in den ursprünglichen embryonalen Zellen gespeichert sind. Auf dieser Grundlage untersuchte das Forscherteam: Was würde passieren, wenn diese lebenden Strukturen mit Nervensystemen „ausgestattet“ würden?
In der neuesten Forschung implantierten Wissenschaftler eine Gruppe neuronaler Vorläuferzellen, die sich zu Neuronen entwickeln werden, in einen im Bau befindlichen biologischen Roboter, um einen sogenannten „Neurobot“ zu bilden. Diese Zellen werden in dem kurzen Zeitfenster eingebettet, in dem sich das kugelförmige Gewebe noch im frühen Entwicklungsstadium befindet, und reifen dann allmählich heran, bilden Dendriten und Axone aus und erstrecken sich ins Innere und an die Oberfläche, um ein einfaches und vollständiges neuronales Netzwerk aufzubauen. Relevante Ergebnisse wurden kürzlich in der Fachzeitschrift Advanced Science veröffentlicht.
Das Projekt, das gemeinsam von Michael Levin, dem Vannevar Bush-Professor für Biologie an der Tufts University, und Haleh Fotowat vom Wyss Institute geleitet wird, ist Teil einer größeren Forschungsanstrengung, um zu verstehen, wie sich Zellgruppen in unbekannten Umgebungen selbst zu komplexen Strukturen organisieren. Die Forscher hoffen, dass diese Art von System „von Grund auf“ die Grundregeln der Bildung und Gestaltung des Nervensystems aufdecken und so eine theoretische Grundlage für die synthetische Biologie und die regenerative Medizin liefern kann, die in Zukunft zum Entwurf neuer biologischer Strukturen oder zur Reparatur beschädigter Gewebe verwendet werden kann.
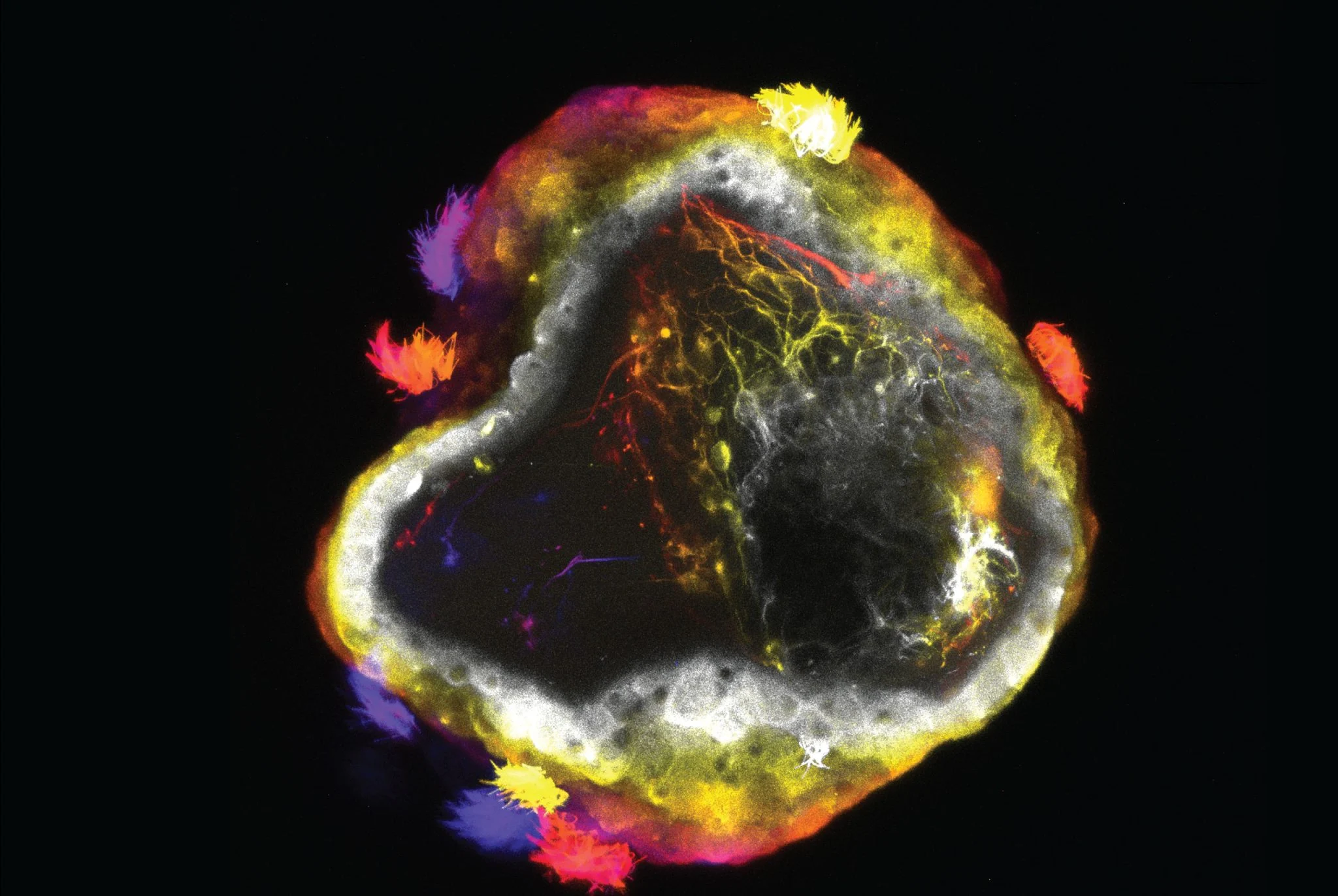
In spezifischen Experimenten isolierte das Team zunächst Vorläufer-Hautzellen aus frühen Xenopus-Embryonen. Diese Zellen aggregieren auf natürliche Weise in einer Kulturschale zu kleinen kugelförmigen Strukturen und ihre Oberflächen sind mit dichten Flimmerhärchen (Zellen mit mehreren Flimmerhärchen) bedeckt. Der koordinierte Schwung der Flimmerhärchen ermöglicht es dem ursprünglichen „Froschzellenroboter“, im Wasser zu schwimmen. Durch das Hinzufügen neuronaler Vorläuferzellen zu dieser Basis hat der entstandene „Neurobot“ seine Form im Vergleich zur Vergangenheit deutlich verändert und ist insgesamt größer und schlanker geworden.
Mikroskopische Beobachtungen zeigten, dass diese eingebetteten Neuronen nicht nur typische dendritische und axonale Strukturen entwickelten, sondern auch synapsenbezogene Proteinmarker exprimierten, was darauf hindeutet, dass Verbindungen zwischen Zellen hergestellt und zur Signalübertragung fähig waren. Mithilfe der Calcium-Bildgebungstechnologie bestätigten die Forscher außerdem, dass die Neuronen im Neuroroboter zu elektrischer Aktivität fähig sind und ein vereinfachtes funktionelles neuronales Netzwerk bilden.
Die Hinzufügung von Nervensystemen verändert auch das Verhalten dieser lebenden Maschinen erheblich. Im Vergleich zu biologischen Robotern ohne Neuronen weisen Neuroroboter häufigere Gesamtaktivitäten und komplexere Bewegungsbahnen auf und zeigen sich wiederholende Bewegungsmuster anstelle einfacher gerader Linien oder zufälliger Spaziergänge. Um die Rolle neuronaler Aktivität im Verhalten zu testen, verwendete das Team Pentylentetrazol, ein Medikament, von dem bekannt ist, dass es die Gehirnaktivität beeinflusst und epileptiforme Reaktionen auslöst, und beobachtete seine Wirkung auf die Bewegung dieser lebenden Strukturen. Die Ergebnisse zeigen, dass das Medikament die Bewegungsmuster von Neurorobotern auf völlig andere Weise verändert als bei biologischen Maschinen, die keine Neuronen enthalten, was darauf hindeutet, dass neu gebildete neuronale Netze das Verhalten dieser „Maschinen“ aktiv beeinflussen.
Fotovat sagte, dass diese Arbeit nicht nur darin besteht, dem biologischen Roboter eine „Steuereinheit“ hinzuzufügen, sondern, was noch wichtiger ist, die inneren Prinzipien der Bildung des Nervensystems umzukehren. Sie wies darauf hin, dass Neuroroboter im Vergleich zur Verfolgung, wie Neuronen an der Entwicklung von Verhaltensweisen bei ausgewachsenen Tieren wie Zebrafischen beteiligt sind, eine Plattform für den Aufbau von Nervensystemen „von Grund auf“ bieten, sodass wir fragen können: „Setzen Sie Neuronen in eine völlig beispiellose Situation, nach welchen angeborenen Regeln werden sie sich in Netzwerken organisieren?“
Levine betonte, dass Neurorobotik eine einzigartige Gelegenheit biete, zu untersuchen, „wie neuronale Netze Bewegung und Verhalten in einem System mit einem Körper beeinflussen“. In traditionellen experimentellen Modellen haben Körper und Nervensystem oft eine lange Geschichte der Koevolution durchlaufen, während Neuroroboter eine völlig neue Kombination ohne evolutionären Hintergrund darstellen, die dabei hilft, Lern- und Evolutionsfaktoren herauszuarbeiten und intuitiv zu beobachten, wie Zellen und Netzwerke in physischen Strukturen zusammenarbeiten.
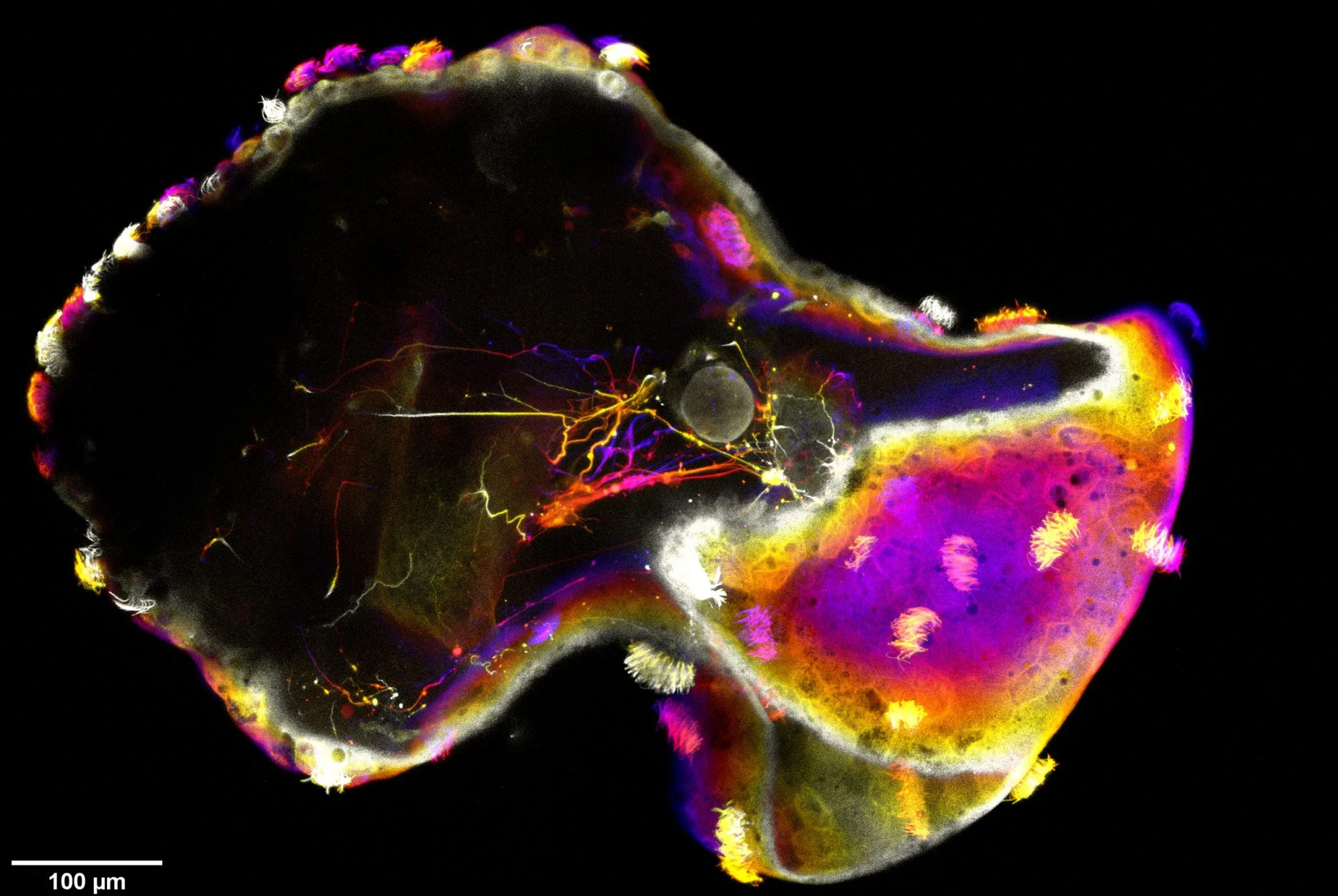
Neben morphologischen und Verhaltensänderungen entdeckten die Forscher auch unerwartete Genexpressionsmuster bei den Neurobots. Zusätzlich zu Genen, die mit wichtigen Gehirnrezeptoren in Zusammenhang stehen, entdeckte das Team auch die Aktivierung einer Reihe von Genen, die an der visuellen Verarbeitung beteiligt sind, darunter Gene, die normalerweise in lichtempfindlichen Zellen im Auge exprimiert werden. Das bedeutet, dass Neuroroboter in Zukunft möglicherweise die Fähigkeit entwickeln, auf Licht zu reagieren, wenn ihre Lebensdauer weiter verlängert und die Kulturbedingungen optimiert werden.
Levin schlug eine zukunftsweisende Hypothese vor: Diese Neuroroboter könnten bestimmte Genmodule „vorregulieren“, die für potenzielle zukünftige Funktionen nützlich sind, als Vorbereitung für die spätere funktionelle Evolution. „Wenn sie länger leben, werden sie dann echte Photorezeptoren weiterentwickeln?“ Er sagte, dies sei eine Frage, die das Team derzeit aktiv erforsche.
Die Forscher wiesen darauf hin, dass man, um mit biologischen Materialien „völlig neue Dinge zu bauen“, zunächst verstehen muss, wie Zellen selbst in unbekannten Umgebungen Probleme lösen und „Entscheidungen“ treffen. Neuroroboter sind eine solche experimentelle Plattform: Sie verfügen über keine etablierten Entwicklungsprogramme und keine durch natürliche Selektion hinterlassenen Strukturvorlagen, zeigen aber dennoch die Fähigkeit, sich selbst zu organisieren, Netzwerke zu bilden und Verhaltensweisen zu erzeugen. Dies stellt nicht nur unser traditionelles Verständnis der Grenze zwischen „Körper“ und „Nervensystem“ in Frage, sondern eröffnet auch die Vorstellungskraft für zukünftige programmierbare lebende Systeme, wie selbstheilende mikromedizinische Geräte und intelligente Komponenten für die Gewebezüchtung.